1) energy level difference of bonding atomic orbitals


成键原子轨道能级差
2) molecular orbital bonding energy


分子轨道成键能
3) nonbonding atomic orbita


非键原子轨道
4) atom orbital energies


原子轨道能
1.
In this paper,the exceptional electron structure of transition elements is better expounded by concept of the atom orbital energies,Hund's rule and relativistic effects.
本文用原子轨道能、洪特规则、相对论性效应的概念较好地解释了过渡元素原子“例外”电子层结
5) bonding MO (BMO)


成键分子轨道
6) energy difference of frontier orbital


前沿轨道能级差
补充资料:原子轨道
| 原子轨道 atomic orbit 描述原子中单电子处于真实的(如氢原子或类氢离子的单电子体系)或假定的(即有效的,如多电子原子的电子体系)中心势场中束缚态波函数的空间部分,即单电子薛定谔方程 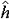 (1)ψ(1)=Eψ(1)的解ψ(1)称原子轨道。式中 (1)ψ(1)=Eψ(1)的解ψ(1)称原子轨道。式中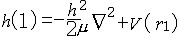 , , 为单电子哈密 顿 算符; μ=mM/(m+M),为约化质量;h=h/2π,h是普朗克常数;▽2是拉普拉斯算符;m、M分别是电子和原子核的质量;V(r)是单电子真实的或假定的有效势函数 ;h(1)和ψ(1)中的数字1表示单电子空间坐标(以核为参考点)。 氢原子和类氢离子是由一个电子和原子核组成的双粒子体系,引入质心坐标以后,求解电子相对于核的相对运动方程,得到电子的波函数ynlm(r,θ,  )=Rnl(r)Ylm(θ, )=Rnl(r)Ylm(θ, ),式中n=1,2,3,…,为主量子数;l=0,1,2,…,-1,为角量子数;m=0,±1,±2,…,±l ,为磁量子数;Rnl(r) 是原子轨道的径向部分;Ylm(θ, ),式中n=1,2,3,…,为主量子数;l=0,1,2,…,-1,为角量子数;m=0,±1,±2,…,±l ,为磁量子数;Rnl(r) 是原子轨道的径向部分;Ylm(θ, )是球谐函数 )是球谐函数,即原子轨道的角度部分。通常用符号s ,p ,d ,f,…等依次代表l=0,1,2,3,…,故 n=2 ,l=0 的状态的原子轨道可写为ψ2s,n=3,l=2的状态可写为ψ3d,余类推。多电子原子轨道通常用自洽场方法求解单电子函数满足的哈特里福克方程获得。 |
说明:补充资料仅用于学习参考,请勿用于其它任何用途。
参考词条