1) ideal solution


理想溶液
1.
In this paper,concepts for the force field condition and shape change of molecules were put forward by deducing relationship between gas phase pressure and molecular force,and therefore a new explanation for the ideal solution was carried out macrocosmically.
本文推演了理想溶液中气相压力与分子间力的关系,提出了力场环境及分子变形的概念。
2.
There are two kinds of standard states for ideal solution.


对于理想溶液 ,可以选择两种标准状态 ,推导了不同标准状态下 ,溶质的化学势表达式 。
2) nonideal solution


非理想溶液
1.
The mathematical model for optimum design of distillation for binary nonideal solution was established, based on the annual cost of distillation system including the distillation column, condensator and reboiler.
建立二元非理想溶液精馏优化设计数学模型 。
3) ideal dilute solution


理想稀溶液
4) nonidcal solution theory


非理想溶液理论
5) Ideal-like solution model


类理想溶液模型
1.
The ideal-like solution model and dilute-like solution model are generalized by the simple rules of thermodynamic properties for the multicomponent systems (A1+A2+.
类理想溶液模型和类稀溶液模型,概括了组元A1、A2、…、Aq的活度恒定条件下,各类多元溶液(A1+A2+…+Aq+B+C+… +Z)相对于其亚系(A1+A2+…+Aq+B)、 (A1+A2+…+Aq+C)、…、 (A1+A2+…+Aq+Z)的热力学性质的简单规律;这些多元溶液广泛应用于冶金学,例如电解质和非电解质的水溶液、有机混合物、固态和液态合金、熔盐、炉渣和非化学计量固态化合物等。
6) partial ideal solution model


偏理想溶液模型
1.
The experimental results showed that their thermodynamic characteristics conform well with the partial ideal solution model and Zdanovskii's rule within the experimental error range, i.
以NaCl和CaCl2水溶液为参考溶液,在298 15K条件下,利用等压法研究了三元轻稀土硝酸盐水溶液{H2O+La(NO3)3+Pr(NO3)3},{H2O+La(NO3)3+Nd(NO3)3}和{H2O+Pr(NO3)3+Nd(NO3)3}及其二元亚系La(NO3)3(aq),Pr(NO3)3(aq)和Nd(NO3)3(aq)溶液的热力学性质·结果表明,在实验误差范围内(≤0 0010),它们的热力学行为符合偏理想溶液模型及Zdanovskii规则
补充资料:理想溶液
| 理想溶液 ideal solution 溶液中的所有组分在全部浓度范围内都严格遵守拉乌尔定律的溶液。同分异构体和有机物中的同系物等都能近似构成理想溶液。在理想溶液中,同种分子的分子间力和异种分子的分子间力平均来说都是相等的,即每一种物质的分子与其他分子的相互作用都与纯态时的相互作用相同。因为理想溶液中的所有组分都服从拉乌尔定律,所以它们的化学势具有完全相同的表示形式:  式中μB为溶液中任一组分B的化学势;T为溶液的热力学温度;p为溶液的压力;xB为B的物质的量分数。 式中μB为溶液中任一组分B的化学势;T为溶液的热力学温度;p为溶液的压力;xB为B的物质的量分数。 为标准压力,习惯上取 为标准压力,习惯上取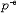 =101.325千帕; =101.325千帕;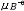 为标准压力下与溶液同温的纯B液体的化学势;Vm,B为纯B的摩尔体积。 为标准压力下与溶液同温的纯B液体的化学势;Vm,B为纯B的摩尔体积。在一定温度和压力下将多种纯液体相混合形成理想溶液,则该过程具有如下特性: ①无热效应,即: ΔminH=0(1)式中ΔminH是上述过程的混合焓。配制理想溶液时不吸收或放出热量,这是由于混合前后无分子间力的变化,使每一种物质在溶液中的偏摩尔焓与纯态时的摩尔焓完全相等,因而整个过程没有焓变。 ②无体积效应,即: ΔmixV=0(2)式中ΔmixV是上述过程的混合体积。配制理想溶液时总体积不发生变化,这是由于每一种物质在溶液中的偏摩尔体积完全等于其纯态时的摩尔体积。 ③混合熵,即: 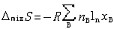 (3)式中ΔmixS是上述过程的混合熵;nB是任一组分B的物质的量;xB是B的物质的量分数;R是摩尔气体常数。 (3)式中ΔmixS是上述过程的混合熵;nB是任一组分B的物质的量;xB是B的物质的量分数;R是摩尔气体常数。④混合吉布斯函数,即: 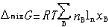 (4)式中ΔmixG是上述过程的混合吉布斯函数。式(1)~(4)表明,理想溶液的配制过程是一个无功、无热、熵增加、吉布斯函数减少的过程。 (4)式中ΔmixG是上述过程的混合吉布斯函数。式(1)~(4)表明,理想溶液的配制过程是一个无功、无热、熵增加、吉布斯函数减少的过程。理想溶液的概念及研究具有重要实际意义和理论价值。在处理任意非理想溶液时总是采用与理想溶液相对比的方法。可通过测量实际溶液的ΔmixH或ΔmixV值,发现它与理想溶液的差异,进而讨论和研究溶液的具体性质和规律。 |
说明:补充资料仅用于学习参考,请勿用于其它任何用途。
参考词条