





一个分子的中心原子究竟采取哪种类型的轨道杂化,直接可以预测整个分子的空间构型。 杂化轨道理论成功地解释了部分共价分子杂化与空间构型关系,但是,仅用杂化轨道理论预测有时是难以确定的。1940年美国的sidgwick nv等人相继提出了价层电子对互斥理论(valence shell electron pair repulsion theory),简 称vsepr法,该法适用于主族元素间形成的abn型分子或离子。该理论认为,一个共价分子或离子中,中心原子a周围所配置的原子b(配位原子)的几何构型,主要决定于中心原子的价电子层中各电子对间的相互排斥作用。这些电子对在中心原子周围按尽可能互相远离的位置排布,以使彼此间的排斥能最小。所谓价层电子对,指的是形成σ键的电子对和孤对电子。孤对电子的存在,增加了电子对间的排斥力,影响了分子中的键角,会改变分子构型的基本类型。根据此理论,只要知道分子或离子中的中心原子上的价层电子对数,就能比较容易而准确地判断 abn 型共价分子或离子的空间构型。
价层电子对理论预测分子空间构型步骤为:
1.确定中心原子中价层电子对数
中心原子的价层电子数和配体所提供的共用电子数的总和除以2,即为中心原子的价层电子对数。 规定:(1)作为配体,卤素原子和h 原子提供1个电子,氧族元素的原子不提供电子;(2)作为中心原子,卤素原子按提供7个电子计算,氧族元素的原子按提供6个电子计算;(3)对于复杂离子,在计算价层电子对数时,还应加上负离子的电荷数或减去正离子的电荷数;(4)计算电子对数时,若剩余1个电子,亦当作 1对电子处理。(5) 双键、叁键等多重键作为1对电子看待。
2.判断分子的空间构型
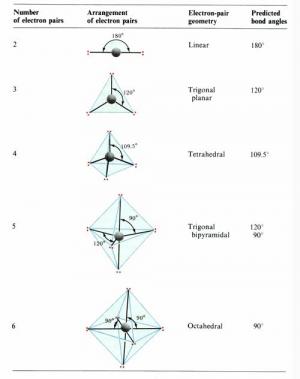
根据中心原子的价层电子对数,从表9-4中找出相应的价层电子对构型后,再根据价层电子对中的孤对电子数,确定电子对的排布方式和分子的空间构型。
实例分析:试判断pcl5 离子的空间构型。
解:p离子的正电荷数为5,中心原子p有5个价电子,cl原子各提供1个电子,所以p原子的价层电子对数为(5+5)/2 = 5,其排布方式为三角双锥。因价层电子对中无孤对电子,所以pcl5 为三角双锥构型。
实例分析:试判断h2o分子的空间构型。
解 :o是h2o分子的中心原子,它有 6个价电子,与o化合的2个h原子各提供1个电子,所以o原子价层电子对数为(6+2)/2 = 4,其排布方式为 四面体,因价层电子对中有2对孤对电子,所以h2o分子的空间构型为v形。
表9-5 理想的价层电子对构型和分子构型
实例分析:判断hcho分子和hcn分子的空间构型
解分子中有1个c=o双键,看作1对成键电子,2个c-h单键为2对成键电子,c原子的价层电子对数为3,且无孤对电子,所以hcho分子的空间构型为平面三角形。
hcn分子的结构式为h—c≡n∶,含有1个c≡n叁键,看作1对成键电子,1个ch单键为1对成键电子,故c原子的价层电子对数为2,且无孤对电子,所以hcn分子的空间构型为直线。