2) colligative properties of dilute solutions


稀溶液的依数性
5) extremely dilute solution properties


极稀溶液性质
6) macromolecule aqueous solutions


水溶性高分子稀溶液
补充资料:依数性
| 依数性 colligativ 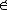 properties properties稀薄理想溶液具有的一组性质。这组性质的值只取决于溶液中溶质分子的含量而与溶质的种类无关,故称为依数性。具体包括蒸气压降低、凝固点降低、沸点升高和渗透压等。 ①蒸气压降低。对于非挥发性溶质的稀薄理想溶液,其蒸气压为: pA= 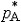 xA= xA=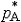 (1-xB) (1-xB)式中pA和 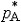 分别为溶液和纯溶剂的蒸气压;xA和xB分别为溶液中溶剂和溶质的物质的量分数。因此非挥发性溶质溶解在溶剂中所引起的蒸气压降低为ΔpA= 分别为溶液和纯溶剂的蒸气压;xA和xB分别为溶液中溶剂和溶质的物质的量分数。因此非挥发性溶质溶解在溶剂中所引起的蒸气压降低为ΔpA=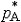 -pA,即: -pA,即:ΔpA= 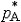 xB (1) xB (1)式中pA为蒸气压降低值 ,可见它只取决于xB而与溶质B的种类无关。 ②凝固点降低。稀薄理想溶液凝固时,若析出的固相是纯态的固体溶剂,则溶液的凝固点Tf将低于纯溶剂的凝固点 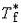 ,即Tf< ,即Tf<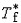 ,且二者之差为: ,且二者之差为: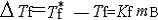 (2) (2)式中Δ 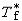 为凝固点降低值 ;mB为溶液的质量摩尔浓度;Kf为凝固点降低常数,其值只与溶剂的性质有关 ,常用溶剂的Kf值可从手册中查得。式(2)表明 ,凝固点降低只与溶质B的含量有关而与其性质无关。 为凝固点降低值 ;mB为溶液的质量摩尔浓度;Kf为凝固点降低常数,其值只与溶剂的性质有关 ,常用溶剂的Kf值可从手册中查得。式(2)表明 ,凝固点降低只与溶质B的含量有关而与其性质无关。③沸点升高。对于含有非挥发性溶质的稀薄理想溶液,由于其蒸气压低于纯溶剂的蒸气压 ,所以其沸点 Tb,必高于纯溶剂的沸点 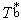 ,即Tb> ,即Tb>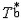 ,且二者之差为: ,且二者之差为: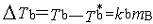 (3) (3)式中ΔTb为沸点升高值;mB是溶液的质量摩尔浓度;Kb为沸点升高常数,其值只与溶剂的性质有关,常用溶剂的Kb值可以从手册中查得。式(3)表明,沸点升高只取决于溶质B的含量而与其性质无关。 ④渗透压。若用只允许溶剂分子通过的半透膜将溶液与纯溶剂隔开,则溶剂分子便会自动地由纯溶剂一侧流向溶液一侧,该现象称为渗透。为了阻止渗透,可在溶液一方施加一额外压力,它称为溶液的渗透压。法国生理学家H.迪特罗1827年首先引入这一概念。1886年范托夫根据实验结果提出了稀薄理想溶液的渗透压公式: Π=cBRT (4) 式中Π是渗透压;cB是溶液的浓度;T是热力学温度;R是摩尔气体常数。式(4)表明,渗透压只取决于溶质B的含量而与其种类无关。 依数性可由实验测定,尤其是凝固点降低和渗透压的测量常被用于确定物质的分子量、检验物质纯度及其他工业用途。 |
说明:补充资料仅用于学习参考,请勿用于其它任何用途。
参考词条